Abstract
Background: Cardiovascular complications of cancer treatment are called cancer treatment-related cardiovascular toxicity (CTCT). Myocardial dysfunction and heart failure are major complications of anti-cancer treatments leading to morbidity and mortality [13]. For this reason, in order to prevent or manage cardiotoxicity without stopping anticancer treatment, the cooperation of specialists who play a role in the treatment of cancer patients is important [15]. It is very difficult to predict the long-term prognosis of cardiovascular system diseases in patients suffering from this pathology. Because cancer patients typically receive combined anticancer chemotherapy and sometimes radiation therapy. Due to the interaction between different forms of treatment, this leads to further increase in cardiotoxicity [10]. Elderly female patients with cardiovascular risk factors are at high risk of developing early heart failure as a result of anticancer chemotherapy [12]. The classification of heart failure caused by cancer treatment was done according to whether the patients were symptomatic or not, and according to the left ventricular ejection fraction index. Symptomatic patients were classified into 4 grades: Very severe - the need for inotropic support or mechanical circulatory support, planning of heart transplantation; Severe - presence of HF-caused hospitalizations; Medium - patients who are being monitored on an outpatient basis and whose need for diuretics is increasing; Mild - patients with mild HF symptoms, but whose condition is stable under appropriate treatment. Asymptomatic patients were classified into 3 levels: Severe - emerging systolic dysfunction (LVEF < 40%); Moderate - new-onset systolic dysfunction, regression to 40-49% with a decrease of ≥10% in LVEF, or new-onset systolic dysfunction with GLS >15% reduction with LVEF<10% reduction and regression to 40-49%, or the presence of cardiac biomarker elevation; Mild - LVEF≥ 50% and 15% decrease in GLS value or new plasma biomarker elevation [2]. The most widely accepted mechanism associated with cardiotoxicity during treatment with anthracyclines is the oxidative stress hypothesis [18]. In general, with all cancer treatments, heart failure typically occurs within days of treatment. Of these, some alkylating drugs such as cisplatin and ifosfamide can rarely cause heart failure with a consistent pathophysiological mechanism related to ischemia. In the patients with preexisting myocardial dysfunction, persistent fluid overload is the cause of the first or recurrent episodes of heart failure, rather than the direct toxicity of these drugs. Docetaxel, a drug more commonly used in breast cancer, increases the likelihood of heart failure when given in combination with or after other anthracyclines, cyclophosphamide, or trastuzumab [11]. Risk-benefit assessment in patients should be performed in such a way that both the individual risk factors of the patients and the potential effect of the treatment are considered together with the characteristics of the tumor [16]. The patients treated with adjuvant anthracyclines should have baseline cardiac function assessed before treatment [5]. At least one cardiac biomarker measurement – high-sensitivity troponin or natriuretic peptide – is conceivable at baseline [4]. Thus, the results of all the studies we examined in the world literature show that it is extremely important to periodically measure cardiac biomarkers during the use of this group of drugs. This article describes the intergroup comparative characterization of the heart failure component of chemotherapy-induced cardiotoxicity with anthracycline-containing combination regimens widely used in the treatment of breast cancer. Aim: The aim of the presented research work is to evaluate the characterization and diagnostic aspects of intergroup heart failure associated with chemotherapy combined with anthracycline-containing regimens in patients with breast cancer. Materials and methods: 20-65 years old 50 and 70 patients (all female, mean age 51.5±0.9 years), who were clinically healthy from a cardiological point of view and underwent chemotherapy combined with anthracycline-containing regimens, diagnosed with breast cancer, were included in the study. During the study, transthoracic echocardiography examination method and cardiac biomarker NT-proBNP results and characteristics of heart failure were prospectively evaluated in all patients before the start of chemotherapy courses and 1 year after the end of the courses. Results: When evaluating the results of clinical observation, transthoracic echocardiography and NT-proBNP examination conducted in patients before the start of chemotherapy courses and 1 year after the end of the courses, violations of the systolic and diastolic functions of the left ventricle were found in most of the patients. Conclusion: Heart failure is a component of cardiotoxicity associated with combination chemotherapy. Transthoracic echocardiography and NT-proBNP can detect early preserved fractional heart failure, thereby enabling early important decision-making.
Full article
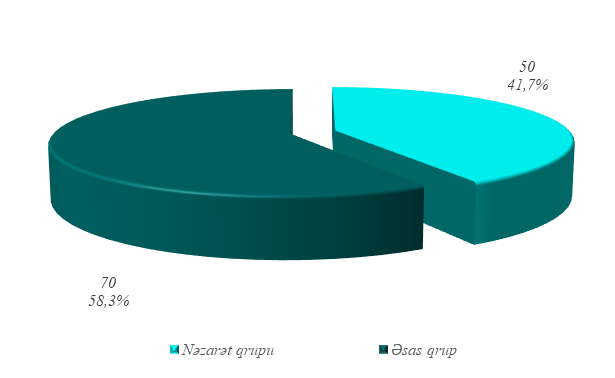
Giriş. Dünyanın inkişaf etmiş ölkələrində xərçəng xəstəliyi səbəbi ilə ölüm ürəyin işemik xəstəlikləri səbəbindən baş verən ölümlərdən sonra ikinci yerdə dayanır. Son illərdə xərçənglə bağlı ölümlərdə stabil azalma müşahidə edilir ki, bu da xərçəngdən sağ qalanların davamlı artması ilə əlaqələndirilir [14]. Son illərdə xərçəng əleyhinə aparılan kimyəvi dərman müalicələrinin proqressiv olaraq inkişafı xərçəng xəstələrinin sağqalmasını artırsada, paralel bir şəkildə əlavə təsirlərinə bağlı olaraq xəstəlik və ölüm faizlərini də artmaqdadır [7]. Belə əlavə təsirlərdən biri, xüsusəndə ən önəmlisi ürək-damar xəstəlikləridir. Xərçəngdən sağalan xəstələrdə əsas xəstəliyin müalicəsinə baglı olaraq, yaranmış ürək-damar xəstəliklərinin bu xəstələrdə ölümlə nəticələnməsi bu gündə öz aktuallığını saxlamaqdadır [6]. Xərçəng əleyhinə müalicə üsullarının belə ciddi kardiotoksikliyi bu müalicə üsullarının ya birbaşa təsiri, ya da ürək-damar xəstəliklərinin risk faktorlarına sahib olan xəstələrdə patoloji prossesləri sürətləndirməsi ilə bağlı ola biləcəyi ehtimal edilir [3]. Bu səbəbdən də, son illərdə kardio-onkologiyaya maraq daha da artmaqdadır. Xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsi ilə əlaqədar olaraq ürək-damar xəstəliklərinin bir çox yönü, xüsusəndə ürək çatışmazlığı ilə ağırlaşması günümüzdə aktual suallarla aydınlaşdırılmanı gözləməkdədir. 2022-ci il Avropa Kardiologiya Cəmiyyətinin (AKC) rəhbər tövsiyələrində bu mövzu səhiyyə sisteminin çox aktual bir problemi olaraq vurğulanıb və həmin tövsiyələrdə həmçinin bu mövzuda gələcəkdə əlavə tədqiqatların aparılması tövsiyə edilmişdir [2].
Aparılmış tədqiqatda (45) əldə edilən məlumatlar göstərir ki, bisoprolol SMAF-da azalmanı zəiflədir və beləliklədə trastuzumabla aparılan xərçəng əleyhinə müalicənin kəsilməsinin əhəmiyyətli dərəcədə qarşısını alır. Müalicədən əvvəl və ya müalicə zamanı ürək funksiyalarındakı pozulmaların aşkarlanması müalicə planının dəyişdirilməsinə və ya zamanında əlavə müdaxilələrə səbəb ola bilər [8].
Süd vəzisi xərçəngi, əsasən Cənubi Şərqi Asiyada, Avstraliya və Yeni Zelandiyada, ümumilikdə isə bütün dünyada qadınlarda rast gəlinən xərçəng patologiyalarının əsas formasıdır [9]. Süd vəzisi xərçənginin müalicəsi şişin estrogen reseptoru, progesteron reseptoru, insan epidermal böyümə faktoru reseptoru-2, xəstəliyin dərəcəsi kimi spesifik markerlərin istifadəsinə əsaslanır. Cərrahiyyə, kimyəvi dərman müalicəsi və şüa terapiyasının hədəflənmiş müalicə ilə birləşdirilməsi ilə demək olar ki, gəlinən nəticə son iyirmi ildə xeyli yaxşılaşmışdır. Bu tədbirlər nəticəsində orta hesabla 5 illik sağqalma hal-hazırda təxminən 87%-dir [9]. Uzun sürən sağqalma, süd vəzisi xərçəngi müalicəsinin hədəfdən kənar təsirlərinə daha çox diqqət yetirilməsinə səbəb oldu. Aydın olmuşdur ki, əslində ürək-damar sistemi fəsadları xəstələrin bir qrupunda xərçənglə əlaqəli ölümləri üstələyə bilər [1].
Xərçəng xəstəliyinin müalicəsindəki inkişaflara bağlı olaraq süd vəzisi xərçəngi xəstələrinində sağqalma müddətinin uzanması, həmçinin bu sahədə yeni tətbiq edilən müalicə vasitələrinin kardiotoksik təsirləri səbəblərindən günlük kardioloji praktikada kardioloqlar xərçəng xəstələri ilə çox sıx qarşılaşmaqdadırlar. Antrasiklinin kardiotoksikliyi barədə məlumatlar əldə olunmağa başlanıldıqdan sonra HER-2 əsaslı müalicələrin formalaşmasına, yanaşı olaraq tirozinkinaza inhibitorlari ilə əlaqəli kardiovaskulyar toksikliklər barədə məlumatlar əldə olunmağa başlanıldıqdan sonra da, ümumulikdə, kardio-onkologiya dissiplininin formalaşmasına səbəb olmuşdur [2].
Material və metodlar. Tədqiqat zamanı xəstələrin araşdırılması iki qrup və hər qrupda iki yarımqrup (hər qrupda yaşı 45 yaşa qədər olan və yaşı 45 yaşdan yuxarı olan xəstələrdən ibarət yarımqruplar) şəklində araşdırılmışdır (qrafik 1).
Tədqiqat qrupu (I qrup) – prospektiv xəstələrdən ibartət olmuş, ilk dəfə süd vəzisi xərçəngi aşkarlanmış 70 nəfər qadın xəstənin məlumatları əsasında təşkil edilmişdir. Bu qrupdakı xəstələr yarımqruplar şəklində (yaşı 45 yaşa qədər olan 21 nəfər xəstə və yaşı 45 yaşdan yuxarı olan 49 nəfər xəstə daxil edilməklə) öyrənilmişdirlər. Bütün xəstələr həm xərçəng əleyhinə müalicəyə başlanlmazdan əvvəl, həm də müalicənin kurslar arası dövrlərində və həmçinin, müalicədən bir il sonrakı dövrdə kardioloji müayinələrdən keçirilmişdirlər.
Nəzarət qrupu (II qrup) – retrospektiv xəstələrdə, kurslar arası dövrlərdə kardioloji müayinələri icra olunmayan süd vəzisi xərçəngi diaqnozu təsdiqlənmiş 50 nəfər qadın xəstənin məlumatları əsasında təşkil edilmişdir. Bu qrupdakı xəstələr də iki yarımqrup (yaşı 45 yaşa qədər olan 10 nəfər xəstə və yaşı 45 yaşdan yuxarı olan 40 nəfər xəstə daxil edilməklə) şəklində öyrənilmişdirlər. Qrupdakı bütün xəstələr də xərçəng əleyhinə müalicəyə başlanılmazdan əvvəl, müalicəni bitirdikdən bilavasitə sonra və müalicəni bitirdikdən bir il sonra ürək fəaliyyətinin qiymətləndirilməsi üçün lazımi kompleks müayinələr aparılmışdırlar. Müayinələr zamanı xəstələr tədqiqatın məqsədinə uyğun olaraq seçilərkən, onların yaşının hansı intervalda dəyişilməsinədə önəm verilmişdir. Belə ki, müayinə olunan xəstələrin məhz 18 yaş ilə 65 yaş aralığında olması əvvəlcədən qarşıya qoyulan seçim kriteriyalarından biri olmuşdır. Ümumilikdə, tədqiqata daxil olan bütün xəstələrin minimal yaş göstəricisi 28 yaş, maksimal yaş göstəricisi 65 yaş və orta yaş göstəricisi isə 51,5±0,9 yaş olmuşdur. Birinci qrupda minimal yaş 28, maksimal yaş 65 və orta yaş göstəricisi isə 51,2±1,2 olmuşdur. İkinci qrup da isə minimal yaş 30, maksimal yaş 65 və orta yaş göstəricisi isə 51,0±1,3 olmuşdur. Cədvəi 1 də tədqiqata daxil edilmiş xəstələrin bütün demoqrafik və klinik göstəriciləri verilmişdir. Cədvəldən də göründüyü kimi qruplar bir-birlərindən yaşa, bədən çəki indeksinə, piylənmə, irsiyyət, siqaret çəkmə və şəkərli diabet kimi risk faktorlarına görə fərqlənməyərək həmcins olmuşdurlar. Qrupların göstəriciləri arasında əldə edilən fərqlər statistik dürüst olmamışdırlar (p>0,05). Tədqiqata daxil edilən xəstələr əvvəlcədən mövcud olan risk faktorlarının xüsusiyyətlərinə görə bir-birlərindən fərqləndirilməyərək hər iki qrupa təsadüfi seçim yolu ilə daxil edilmişdirlər.
Nəticələrin müzakirəsi. Xəstələrdə kimyaterapiya kurslarına başlanılmazdan əvvəl və kurslar bitdikdən 1 il sonra aparılmış klinik musahidə, transtorakal exokardioqrafiya və NT-PROBNP müayinəsinin nəticələri dəyərləndirildikdə xəstələrin əksəriyyətində sol mədəciyin sistolik və diastolik funksiyalarının pozulması aşkarlanmışdır. Xərçəng diaqnozu qoyulmuş xəstələr də biomarkerlər (troponin və NT-proBNP) ürək damar sistemində mövcud ola biləcək risk səviyyəsini dəqiqləşdirmək üçün istifadə edilə bilər. Belə ki, biomarkerlər sol mədəciyin atım fraksiyasındakı bazal dəyərələrdə azalmaların baş verməsindən daha əvvəl sol mədəciyin sistolik və diastolik disfunksiyalarının subklinik əlamətlərini askarlaya bilərlər. Troponin yüksəkliyinin aparılan kimyəvi dərman müalicəsinin ağırlaşma yaratma riskinin yüksəkliyi ilə əlaqəli olduğuna dair bəzi sübutlar askarlanmaqdadır. Bu səbəbdən də, ilkin troponin səviyyəsi yüksək olan xəstələrdə daha sıx aralıqlarla ölçülməlidir. Yüksək doza kimyəvi dərman müalicəsindən sonra artan troponin ilə müalicədən sonra yarana biləcək ürək damar patologiyaları arasında bir əlaqə mövcud olduğu düşünülməkdədir. NT-proBNP-nin davamlı yüksəlməsi isə, aşkar olaraq ürək çatışmazlığının yaranma riskinin artmasını göstərən bir parametrdir. Bizim tədqiqatımız zamanı da ürək çatışmazlığının diaqnotikasında önəmli rol oynayan biomarkerlərdən biri olan NT-proBNP-nin davamlı kontrolu aparılmışdır. Bu da bizə ürək çatışmazlığının aşkarlanmasında çox əhəmiyyətli dərəcədə fayda vermişdir. Xüsusən sol mədəciyin diastolik disfunksiyası yaranmış xəstələrimizdə nəçə faizində eyni zamanda diastolik ürək çatışmazlığının yaranmasını təyin etməkdə tədqiqatımızın önəmli diaqnostik meyarı olmuşdur [13]. Tədqiqatımız zamanı kontrol müyinələrin 1 il sonrakı nəticələrinin müqayisəsi zamanı retrospektiv olaraq araşdırılan qrupa daxil olan xəstələrimizdə NT-proBNP-nin səviyyəsi daha yüksək olmuşdur ki, bunu da həmin qrupa daxil olan xəstələrdə kurslar arası dövr də lazımi kontrol müayinələrin aparılmaması ilə əlaqələndirmək olar. Nəzarət qrupu xəstələrin xərçəng əleyhinə aparılan kimyəvi dərman müalicəsindən 1 il sonrakı kontrol müayinələri zamanı xəstələrdə laborator müayinələrdən qanda NT pro-BNP səviyyəsinin təyin edilməsi zamanı bu parametrin qrup üzrə orta göstərici 1126,4±100,7 pg/ml olmuşdur. Əsas tədqiqat qrupu xəstələrində isə 3-cü kurs xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsindən sonra bu qrupa daxil olmuş xəstələrdən cəmi 1 nəfər xəstədə NT-proBNP səviyyəsi yüksəlmişdir. Bu qrupda 4-cü kurs xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsindən sonra isə 40 nəfər xəstədə isə NT-proBNP səviyyəsi yüksəlmişdir. 5-ci kurs müalicə sonrası isə qrupa daxil olan 5 xəstədə NT-proBNP səviyyəsi yüksəlmişdir. Tədqiqatın prospektiv araşdırılan əsas qrupunda 21 nəfər xəstə 6 kurs xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsi almışdır. 6-cı kurs xərçəng əleyhinə kimyəvi dərman müalicəsindən sonra xəstələrin 8 nəfərində NT-proBNP səviyyəsi yüksəlmişdir. Bu qrupdan olan 10 nəfər xəstə 7 kurs xərçəng əleyhinə kimyəvi dərman müalicəsi almışdır. 7-ci kurs xərçəng əleyhinə kimyəvi dərman müalicəsindən sonra cəmi 2 nəfər xəstədə isə NT-proBNP səviyyəsi yüksəlmişdir. Əsas qrupa daxil olan xəstələrin xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsinin 8-ci kursundan sonrakı kontrol müayinələri zamanı NT-proBNP səviyyəsi 17 nəfər xəstədə normadan yüksək səviyyədə olmuşdur. Bu qrupa daxil olan xəstələrin xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsindən 1 il sonrakı kontrol yoxlamaları zamanı bütün xəstələrdə qanda NT pro-BNP səviyyəsi təyin edilmişdir. 1 il sonra bu parametrin qrup üzrə orta göstərici 501,0±27,1 pg/ml olmuşdur (pW<0,001).
Exokardiografiya bütün onkoloji xəstələrdə ürək damar sisteminin dəyərləndirilməsində çox önəmli instrumental müayinə üsuludur. Belə ki, ürək damar sistemində yarana biləcək pozğunluqlara qarşı qoruyucu dərmanların vaxtında başlanılması sol mədəciyin atım fraksiyasının yaxşılaşma ehtimalını artırır və yaranan pozğunluqların inkişaf sürətini azalda bilər [13]. Bizim araşdırmamız zamanıda exokardiografiya müayinə üsulundan geniş istifadə etmişik. Bütün müalicə kurslarından sonra exokardiografiya müayinəsinin aparılması bizə ürək çatışmazlığının vaxtında aşkarlanması üçün əhəmiyyətli məlumatlar vermişdir. Beləki, əsas qrupdan olan xəstələrdən 40 nəfərində xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsinin 4-cü kursundan sonra qorunmuş atım fraksiyalı ürək çatışmazlığı yarandığı aşkarlanmışdır. Bu qrupda xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsinin 8-ci kursundan sonra isə xəstələrin əksəriyyətində qorunmuş atım fraksiyalı ürək çatışmazlığı yarandı.
Tədqiqatımızın əsas qrupunda exokardioqrafiya müayinəsi və biomarkerlərin təyin edilməsi zamanı, ürək damar sistemində pozulmalar baş vermiş xəstələrdə zamanında aparılmış müalicə tədbirləri (AÇFİ və beta blokatorlar ilə) nəticəsində nəzarət qrupuna nisbətən daha üstün nəticələr əldə olunmuşdur.Tədqiqatımız zamanı da əsas qrupda bütün kurslar arasında aparılmış kontrol müayinələr və onların nəticələrinə bağlı olaraq ürək çatışmazlığına aid vaxtında aparılmış müalicələr nəticəsində nəzarət qrupuna nisbətən daha az ürək çatışmazlığı yaranmışdır. Beləki, xərçəng əleyhinə aparılmış kimyəvi dərman müalicəsindən 1 il sonra nəzarət qrupuna daxil olan xəstələr arasında 36,6% qorunmuş atım fraksiyalı ürək çatışmazlığı, 54,0% mülayim atım fraksiyalı ürək çatışmazlığı, 5,0% isə azalmış atım fraksiyalı ürək çatışmazlığı yaranmışdır. Tədqiqatımızın əsas qrupuna daxil olan xəstələr arasında isə 52,0% qorunmuş atım fraksiyalı ürək çatışmazlığı və 12,9% mülayim atım fraksiyalı ürək çatışmazlığı yaranmışdır. Beləki, əsas qrupda ürək çatışmazlığı daha zəif inkişaf etmişdir.
Yekun: Ürək çatışmazlığı kombinə olunmuş kimyaterapiyaya bağlı yaranan kardiotoksikliyin bir komponentidir. Transtorasik exokardioqrafiya və NTPROBNP ilə erkən olaraq qorunmuş atım fraksiyalı ürək çatışmazlığı askarlana bilər ki, bunulada erkən önəmli qərarlar alınmasını təmin etmək mümkündür.
Figures
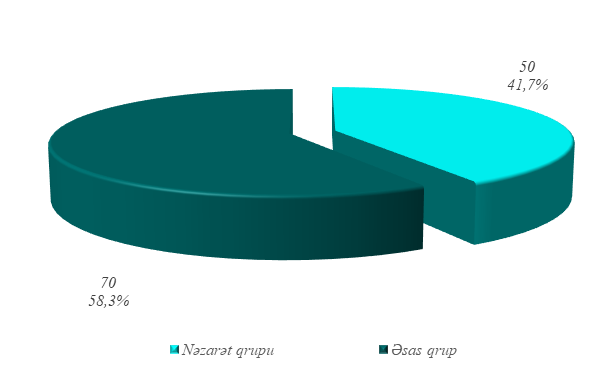
Keywords
References
1. Abdel-Qadir H. A population-based study of cardiovascular mortality following early-stage breast Cancer / H. Abdel-Qadir, P.C. Austin, D.S. Lee [et al.] // JAMA Cardiol, - 2017. v. 2, no 1, - p. 88–93.
2. Alexander R.L. 2022 ESC Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS) / R.L. Alexander, L.F. Teresa, S.C. Liam [et al.] //
Eur Heart J, - 2022. v. 43, no 41, - p. 4229-4361.
3. Armstrong G.T. Modifiable risk factors and major cardiac events among adult survivors of childhood cancer / G.T. Armstrong, K.C. Oeffinger, Y. Chen [et al.] // J Clin Oncol, - 2013. v. 31, p. 3673–3680.
4. Cardinale D. Role of biomarkers in chemotherapy-induced cardio- toxicity / D. Cardinale, M.T. Sandri // Prog Cardiovasc Dis, - 2010. v. 53, p. 121–129.
5. Drafts B.C. Low to moderate dose anthracycline-based chemotherapy is associated with early noninvasive imaging evidence of subclinical cardiovascular disease / B.C. Drafts, K.M. Twomley, R.Jr. D’Agostino // JACC Cardiovasc Imaging, - 2013. v. 6, p. 877 –885.
6. Ewer M.S. Cardiotoxicity of anticancer treatments / Ewer M.S. // Nat Rev Cardio, - 2015. v.12, p. 620.
7. Ferlay J. Cancer incidence and mortality patterns in Europe: estimates for 40 countries in 2012 / J.Ferlay, E. Steliarova-Foucher, J. Lortet-Tieulent [et al.] // Eur J Cancer, - 2013. v. 49, p. 1374–1403.
8. Henriksen P.A. Anthracycline cardiotoxicity: an update on mechanisms, monitoring and prevention / P.A. Henriksen // Heart, - 2017.v. 2, p. 89.
9. https://gco.iarc.fr/today. Accessed 30 June 20.
10. Khouri M.G. Cancer therapy-induced cardiac toxicity in early breast cancer: addressing the unresolved issues / M.G. Khouri, P.S. Douglas, J. R. Mackey [et al.] // Circulation, - 2012. v.126, p. 2749 – 2763.
11. Mackey J.R. Adjuvant docetaxel, doxorubicin, and cyclophosphamide in node-positive breast cancer: 10-year follow-up of the phase 3 randomised BCIRG 001 trial / J.R. Mackey, M. Martin, T. Pienkowski [et al.] // Lancet Oncol, - 2013. v. 14, p. 72 –80.
12. Mehta L.S. Cardiovascular Disease and Breast Cancer: Where These Entities Intersect: A Scientific Statement From the American Heart Association / L.S. Mehta, K.E. Watson, A. Barac [et al.] // Circulation, - 2018. v. 137, no 8, e30–e66.
13. Rebecca D. BSE and BCOS Guideline for Transthoracic Echocardiographic Assessment of Adult Cancer Patients Receiving Anthracyclines and/or Trastuzumab / D. Rebecca, K.G. Arjun, K. Bonnie [et al.] // JACC: CARDIOONCOLOGY, -2021. v. 3, no 1, p. 1-16.
14. Sung H. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries / H.Sung, J. Ferlay, R.L. Siegel [et al.] // CA Cancer J Clin, - 2021. v. 71, p. 209–249.
15. Suter T.M.Cancer drugs and the heart: importance and management / T.M. Suter, M.S. Ewer // Eur Heart J, - 2013. v. 34, p. 1102 –1111.
16. Yu A.F. Trastuzumab interruption and treatment-induced cardiotoxicity in early HER2-positive breast cancer / A.F. Yu, N.U. Yadav, B.Y. Lung [et al.] // Breast Cancer Res Treat, - 2015. v. 149, p. 489–495.
17. Zamorano J.L. 2016 ESC Position Paper on cancer treatments and cardiovascular toxicity developed under the auspices of the ESC Committee for Practice Guidelines / J.L. Zamorano, L. Patrizio, A. Victor [et al.] // European Heart Journal, - 2016. v. 37, p. 2768–2801.
18. Zhang S. Identification of the molecular basis of doxorubicin-induced cardiotoxicity / S. Zhang, X. Liu, T. Bawa-Khalfe [et al.] // Nat Med, - 2012. v. 18, p. 1639 –1642.
Article Info:
Publication history
Published: 28.Jun.2025
Copyright
© 2013-2025. Azerbaijan Society of Cardiology. Published by "Uptodate in Medicine" health sciences publishing. All rights reserved.Related Articles
Viewed: 14


